液相多肽合成(solution phase synthesis) 原理
基于将单个N-α保护氨基酸反复加到生长的氨基成份上,合成一步步地进行, 通常从合成链的C端氨基酸开始,接着的单个氨基酸的连接通过用DCC,混合炭酐, 或N-carboxy酐方法实现。Carbodiimide方法包括用DCC做连接剂连接N-和C-保护氨基酸。重要的是, 这种连接试剂促接N保护氨基酸自己炭基和C保护氨基酸自由氨基间的缩水,形成肽链, 同时产出副产物。 然而, 此方法因其导致消旋的副反应,或在强碱存在时形成5(4H)-oxaylones和N-acylurea而受到影响。庆幸地是, 这些副反应能最小化,如果还不能完全消除。方法是加入像HoSu或HoBT这样的连接催化剂, 此外,此方法也可用于合成N保护氨基酸的活性酯衍生物。依次产生的活性酯将自发与任何别的C保护氨基酸或肽反应形成新的肽。
液相多肽合成现在仍然广泛的使用,液相多肽合成在合成短肽和多肽片段上具有合成规模大,合成成本低的显著优点,而且由于是在均相中进行反应,可以选择的反应条件更加丰富,像一些催化氢化,碱性水解等条件,都可以使用,这在固相中,使用却由于反应效率低,以及副反应等原因,无法应用。液相多肽合成中主要采用BOC和Z两种反应策略。
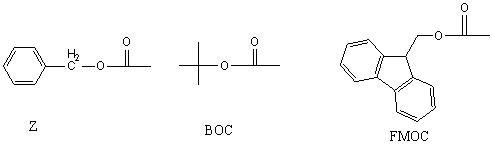
液相合成Glu-Trp 示意图
缩合试剂主要有:碳二亚胺型,鎓盐型(Uronium)
碳二亚胺型
主要包括:DCC,DIC,EDC.HCl等。采用DCC进行反应,由于反应中生成的DCU,在DMF中溶解度很小,产生白色沉淀,所以一般不用在固相合成中,但是由于其价格便宜,在液相合成中,可以通过过滤除去,应用仍然相当广泛。EDC.HCl因为其水溶解性的特点,在多肽与蛋白的连接中使用比较多,而且也相当成功。但是该类型的缩合试剂的一个最大的缺点,就是如果单独使用,会有比较多的副反应,但是在多肽合成的研究表明如果在活化过程中添加HOBt,HOAt等试剂,可以将其副反应控制在很低的范围。
鎓盐型
鎓盐型缩合试剂反应活性高,速度快,现在使用非常广泛,主要包括:HBTU,TBTU,HATU,PyBOP等。该试剂使用过程中需要添加有机碱,如,二异丙基乙胺(DIEA),N-甲基吗啉(NMM),该试剂加入后,才能活化氨基酸。
液相反应特点:
大多数的经典化学反应都是在溶液中进行的。 因此:
(1)在溶液相合成中,可以使用先前所有的有机合成方法而没有任何的限制;
(2)反应物均一混合并且快速移动使得反应机会增加;
(3)在加热反应的例子中,热能通过溶液中的分子分散而被均匀转移;
(4)大量反应可以通过控制反应釜的大小和反应物的数量而实现;
(5)可以在每个步骤提纯并且分析反应化合物。
缺点:
(1)在反应完成之后,需要的化合物和副产物都一起在反应混合物中,需要溶液化学中的分离步骤。
(2)如果使用过量试剂以获得高产量,需要提纯试剂。
(3)如果起始物质或副产物(或需要的化合物)易挥发或沉淀,那就容易多了,可是,如果这些不发生,就需要一个比较困难的后处理工作-萃取或色谱。 因此,后处理过程通常需要更多的时间和精力胜于反应过程。
(4)自动化溶液相合成由于提纯程序的复杂化而非常困难,因而难以实现